5月全球最新獲批藥品和器械盤點
聲明:本文為火石創造原創文章,歡迎個人轉發分享,網站、公眾號等轉載需經授權
摘要
2023年5月,全球批準新藥數量大幅增長。FDA批準19款新藥(NDA/BLA),包含6款新獲批的新分子實體藥物(NDA:Type 1 - New Molecular Entity),3款生物制品藥物(BLA);EMA新授權6款藥品上市,包含0款新活性物質;NMPA批準4個品規(3個品種)創新藥上市,其中3個品規(2個品種)化藥,1個品規(1個品種)生物制品。
醫療器械方面,FDA通過3個上市前批準(PMA)途徑首次上市的產品。境內公示了4個三類醫療器械進入創新審批綠色通道,批準了3個創新器械上市,國內醫療器械審批集中在體外診斷試劑,共1040項,占33.56%。
01
全球藥品獲批情況
(一)美國FDA批準情況

圖1 2022年5月—2023年5月FDA藥物批準數量變化情況
來源:美國食品藥品監督管理局
如圖1,截至2023年6月8日FDA官網披露,2023年5月FDA共完成81項藥品首次批準(不包含暫時批準),其中NDA/BLA批準19款(不包含暫時批準),見表1。其中包括6款新獲批的新分子實體藥物(NDA:Type 1 - New Molecular Entity),3款生物制品藥物(BLA)。
安斯泰來公司的口服藥物VEOZAH是首款獲FDA批準用以治療由更年期引起的中度至重度血管運動癥狀的神經激肽3受體拮抗劑,曾獲優先審評資格;MIEBO是FDA批準的首個也是唯一一個直接針對淚液蒸發的干眼癥治療方法;EPKINLY用于治療復發或難治性彌漫性大B細胞淋巴瘤,是首款獲FDA批準治療DLBCL患者的雙特異性抗體療法;XACDURO是一款靜脈輸注的復方藥物,是首個被批準用于治療由不動桿菌引起的醫院獲得性和呼吸機相關肺炎的病原體靶向療法;輝瑞公司的口服抗新冠病毒藥物PAXLOVID是FDA批準的第四種用于治療成人COVID-19的藥物,也是唯一一款口服抗病毒藥。POSLUMA用于前列腺癌男性前列腺特異性膜抗原陽性病變男性患者的正電子發射斷層掃描,是首個用于前列腺癌的放射性雜交PSMA靶向PET顯像劑。表1 2023年5月FDA批準NDA/BLA藥物列表

來源:美國食品藥品監督管理局
(二)歐盟EMA批準情況
截至2023年6月8日EMA官網披露,2022年5月至2023年5月的推薦上市藥品及新活性物質(NAS)數量情況見圖2,2023年5月EMA未推薦藥品上市。

圖2 2022年5月—2023年5月EMA推薦上市藥品數量變化情況
來源:火石創造產業數據中心
截至2023年6月8日,EMA在5月新授權6款藥品上市,其中包括0款新活性物質,見表2。
表2 2023年5月EMA授權藥物列表

來源:火石創造產業數據中心
(三)NMPA批準情況
截至2023年6月8日NMPA披露,2023年5月共批準國產首次注冊藥品109件。按劑型去重后,共78個藥品品種(不同廠家生產同一藥物按同一品種計算)。本月有4個品規(3個品種)1類創新藥獲批,其中3個品規(2個品種)為化藥,1個品規(1個品種)為生物制品。2023年5月NMPA批準的1類創新藥情況見表3。
表3 NMPA批準的1類創新藥獲批列表

來源:國家藥品監督管理總局
南京圣和藥業自主研發并擁有自主知識產權的奧磷布韋片是國內首個擁有自主知識產權的泛基因型非結構蛋白5B(NS5B)抑制劑,適用于與鹽酸達拉他韋聯用,治療初治或干擾素經治的基因1、2、3、6型成人慢性丙型肝炎病毒(HCV)感染,該藥品的上市為非小細胞肺癌患者提供了新的治療選擇;
浙江博銳生物申報的澤貝妥單抗注射液適用于CD20(B淋巴細胞表面攜帶的一種分子標記物)陽性彌漫大B細胞淋巴瘤,該藥是國內首個獲批上市的國產CD20抗體1類新藥,也是博銳生物首款獲批上市的1類創新生物藥,該品種的上市為淋巴瘤患者提供了更多的治療選擇;
貝達藥業申報的甲磺酸貝福替尼膠囊適用于既往經表皮生長因子受體(EGFR)酪氨酸激酶抑制劑治療出現疾病進展,并且伴隨EGFR T790M突變陽性的局部晚期或轉移性非小細胞肺癌患者的治療,是針對T790M突變的第三代EGFR-TKI,具有巨大的臨床需求,2018年12月,貝達藥業與益方生物達成合作,獲得貝福替尼在中國大陸、香港和臺灣地區的權益,并可獨家在合作區域內進行該產品的開發及商業化,該產品是貝達藥業第5款獲批上市的創新藥。
(四)仿制藥一致性評價情況
截至2023年6月8日CDE官網披露,CDE共承辦藥品一致性評價受理號4892個,2023年5月共新增承辦62個受理號。截至2023年6月8日,共5989個品規上市藥品通過一致性評價(包含視同通過2699個品規),本月共84個品規的藥品通過一致性評價(包含視同通過14個品規),按劑型去重后,共55個藥品品種。目前一致性評價品種通過的注射劑共2383個品規(313個品種),本月過評藥品中共計50個品規(28個品種)的注射劑。2022年5月至2023年5月通過一致性評價數量見圖3。

圖3 2022年5月—2023年5月仿制藥一致性評價批準數量變化情況
來源:國家藥品監督管理總局
02
全球醫療器械獲批情況
(一)美國FDA批準情況
截至2023年6月8日,5月FDA共批準267個510(k)途徑的產品,其中一類器械15個,二類器械246個,未分類6個。通過對510(k)上市前通知的器械根據美國醫學專業用途進行分類,結果發現,5月產品獲批類型最多的為骨科器械、放射科器械、一般和整形手術器械、心血管器械與一般醫院和個人使用類器械,見圖4。
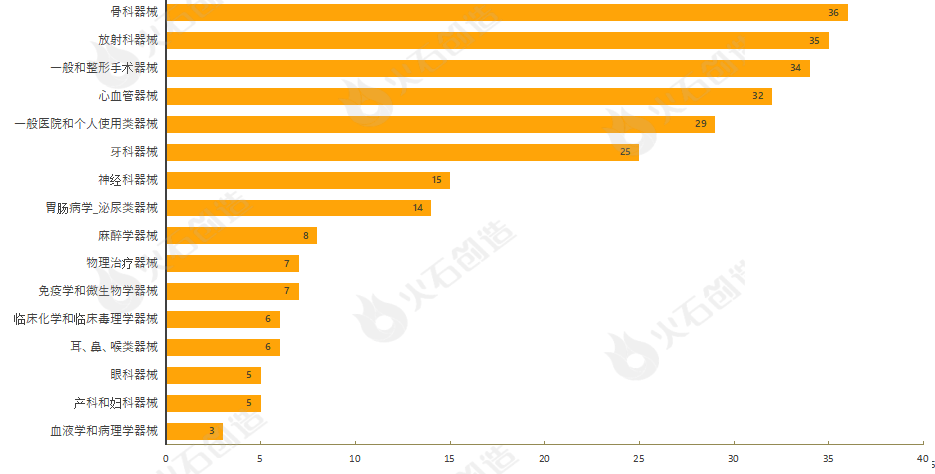
圖4 2023年5月通過FDA 510(k)途徑獲批上市產品類型分布情況
來源:美國食品藥品監督管理局
2023年5月有3個通過上市前批準(PMA)途徑首次上市的產品。
表4 2023年5月PMA首次批準的器械

來源:美國食品藥品監督管理局
(二)境內批準情況
截至2023年6月8日,2023年5月國家局公示了4個三類醫療器械進入創新審批綠色通道,見表5。
表5 2023年5月進入綠色通道的三類創新器械

來源:國家醫療器械審評中心
截至2023年6月8日,2023年5月國家局公示了3個三類創新器械獲批上市,見表6。
表6 2023年5月獲批上市的三類創新器械

來源:國家醫療器械審評中心
截至2023年6月8日,2023年5月國家局共批準首次注冊三類醫療器械產品185個,其中國產156個,進口29個。各省級藥品監管部門5月共批準國產第二類醫療器械注冊771個,一類備案醫療器械2143個。統計數據顯示,體外診斷試劑數量最多,共1040項,占33.56%,基本上均為國產,為1027項。除體外診斷試劑,批準注冊類別數量排前三位的分別為注輸、護理和防護器械、無源手術器械,口腔科器械。表7 5月國產、進口醫療器械批準注冊類別數目分布情況

來源:國家醫療器械審評中心
從地域分布上,2023年5月國產二、三類注冊產品批件最多的依次為江蘇省(168件)、廣東省(139件)、北京市(94件)三個區域,見圖5。

圖5 國產獲批器械區域分布
來源:火石創造產業數據中心
—END—
作者 | 火石創造 王歡 審核 | 火石創造 劉輝興 殷莉
原文標題 : 5月全球最新獲批藥品和器械盤點

請輸入評論內容...
請輸入評論/評論長度6~500個字
圖片新聞







 分享
分享












