FDA
-

-

FDA開啟“實(shí)時(shí)模式”:大藥企加速,Biotech承壓
新藥研發(fā)的游戲規(guī)則,正在悄悄換擋。 過去,藥企像是參加一場(chǎng)漫長(zhǎng)的閉卷考試:試驗(yàn)做完,數(shù)據(jù)收齊,清洗分析,材料裝訂,最后遞到FDA面前。監(jiān)管方到終點(diǎn)“收卷”,再判斷成績(jī)好不好。 現(xiàn)在,F(xiàn)DA想提前進(jìn)考場(chǎng)
FDA、生物制藥 2026-04-30 -
2026年第二季度FDA關(guān)鍵審批決策前瞻
隨著2026年第二季度的臨近,美國食品藥品監(jiān)督管理局(FDA)將就數(shù)項(xiàng)備受矚目的創(chuàng)新療法做出審批決定,這些決定有望為高血壓、肥胖癥及特定乳腺癌患者帶來新的治療選擇。其中,三種關(guān)鍵的候選藥物——baxd
-

股價(jià)大跌19%!FDA拒絕批準(zhǔn)一款基因療法
2026年2月9日,Regenxbio公司宣布,美國FDA以試驗(yàn)設(shè)計(jì)存在不確定性為由,拒絕批準(zhǔn)其用于治療罕見病亨特氏綜合征的基因療法。 Regenxbio的股價(jià)在盤后交易中暴跌約19%,跌至8.31美
-

2025年FDA新藥審批盤點(diǎn)
-01- 引言 盡管經(jīng)歷了內(nèi)部人事動(dòng)蕩與政策調(diào)整,美國食品藥品監(jiān)督管理局在2025年依然保持了活躍的審批節(jié)奏。其藥品評(píng)價(jià)與研究中心共批準(zhǔn)了46種新治療藥物,盡管這一數(shù)字將五年平均值略微拉低至每年48種
-

醫(yī)療器械產(chǎn)品獲FDA許可!九安醫(yī)療“破凈”突圍?
九安醫(yī)療產(chǎn)品獲FDA許可,這能否成為其打破‘破凈’僵局的關(guān)鍵一步? 2025年12月14日,一則看似尋常的獲批公告,可以說為深陷“破凈”泥潭的九安醫(yī)療投下了一縷微光。 天津九安醫(yī)療電子股份有限公司(以
-

-

FDA授予石藥合作伙伴Corbus Nectin-4 ADC快速通道資格
2025年9月16日,Corbus Pharmaceuticals宣布,美國FDA已授予其Nectin-4 ADC CRB-701快速通道資格,用于治療既往接受過鉑類化療及抗PD(L)-1療法后復(fù)發(fā)或
-
當(dāng)FDA超級(jí)加倍重視OS
在腫瘤藥物研發(fā)領(lǐng)域,總生存期(OS)始終是衡量藥物療效的“金標(biāo)準(zhǔn)”。這一指標(biāo)直接關(guān)聯(lián)患者“活得更久”的核心需求,是藥物臨床價(jià)值最直觀的體現(xiàn)。 但基于客觀現(xiàn)實(shí)——為讓患者更快用上新藥,過去十余年間,F(xiàn)D
-

剛剛!全球首個(gè)DPP1抑制劑獲FDA批準(zhǔn)上市
2025年8月12日,Insmed宣布,F(xiàn)DA正式批準(zhǔn)其DPP1抑制劑brensocatib上市,用于治療12歲及以上兒童和成人非囊性纖維化支氣管擴(kuò)張癥患者。 這標(biāo)志著該疾病領(lǐng)域迎來首款靶向治療藥物,
-
FDA改朝,溶瘤病毒遭殃?
一紙完整回復(fù)函(CRL),讓Replimune市值一夜蒸發(fā)近8成,也讓整個(gè)溶瘤病毒領(lǐng)域感受到了FDA監(jiān)管風(fēng)向轉(zhuǎn)變所帶來的刺骨寒意。 就在7月22日,Replimune宣布其溶瘤病毒RP1聯(lián)合PD-1治
-
FDA揭開藥企“遮羞布”
FDA 的一則舉動(dòng)引發(fā)藥圈轟動(dòng)。 7月10日,F(xiàn)DA 一次性公布了202封完整的回復(fù)函(CRL),涵蓋2020年至2024年間最終獲批的202個(gè)藥物。 CRL是對(duì)藥物批準(zhǔn)請(qǐng)求的拒絕,可能出于多種原因而
-
中國創(chuàng)新藥被FDA拒絕的真相
7月10日,F(xiàn)DA公布了202封完整的回復(fù)函(CRL),針對(duì)2020年至2024年期間提交給FDA藥品或生物制品的審批申請(qǐng)。 所有CRL均詳細(xì)說明了藥品未通過的原因及建議。對(duì)此,F(xiàn)DA局長(zhǎng)Marty
-

美國FDA批準(zhǔn)再生元BCMA/CD3雙抗治療多發(fā)性骨髓瘤
2025年7月2日,美國FDA宣布,加速批準(zhǔn)再生元制藥(Regeneron)研發(fā)的linvoseltamab-gcpt(商品名:Lynozyfic)上市,用于治療既往接受至少四線治療的復(fù)發(fā)或難治性多發(fā)
-

重大信號(hào)!FDA擬削減PDUFA費(fèi)用,并加快藥物審批
據(jù)外媒報(bào)道,美國FDA局長(zhǎng)Martin A. Makary近日表示,F(xiàn)DA正醞釀一場(chǎng)深刻變革:FDA正在探索多種方式以加快藥物審批流程,并考慮削減用戶費(fèi)用,以降低藥企負(fù)擔(dān),推動(dòng)創(chuàng)新藥物更快上市。
-
2025年FDA新藥申請(qǐng)費(fèi)漲430萬美元;藥明巨諾任命新總裁
FDA再次提高費(fèi)用。 最近,F(xiàn)DA宣布,對(duì)于2025財(cái)年提交包含臨床數(shù)據(jù)的新藥和生物制劑申請(qǐng)的公司,將需要支付430萬美元的費(fèi)用,比2024財(cái)年增加了約30萬美元。 對(duì)于不需要提交臨床數(shù)據(jù)的申請(qǐng),費(fèi)用從上一年的160萬美元上升至今年的200萬美元,并預(yù)計(jì)在2025年將增至220萬美元
-
腸癌血檢產(chǎn)品獲FDA批準(zhǔn)上市;默沙東、輝瑞發(fā)布財(cái)報(bào)
結(jié)直腸癌早篩市場(chǎng)迎來新成員。 7月29日,Guardant Health宣布,美國FDA已批準(zhǔn)其Shield™血液檢測(cè)技術(shù),用于45歲及以上成年人的結(jié)直腸癌篩查,特別是針對(duì)那些處于平均風(fēng)險(xiǎn)水平的人群
-
研發(fā)黑洞的世紀(jì)分歧,EMA給FDA投了反對(duì)票
在醫(yī)療監(jiān)管的舞臺(tái)上,美國食品藥品監(jiān)督管理局(FDA)和歐洲藥品管理局(EMA)是兩大權(quán)威機(jī)構(gòu)。 它們以各自的審慎態(tài)度和嚴(yán)格標(biāo)準(zhǔn),對(duì)新藥的安全性和有效性進(jìn)行嚴(yán)格把關(guān)。當(dāng)然,在某些藥物審批上,它們也會(huì)出現(xiàn)明顯的分歧
-
全國醫(yī)療保障標(biāo)準(zhǔn)化工作組成立;FDA授予現(xiàn)貨型T細(xì)胞療法優(yōu)先審評(píng)資格
7月18日,全國醫(yī)療保障標(biāo)準(zhǔn)化工作組在北京成立。 據(jù)了解,目前我國醫(yī)療保障標(biāo)準(zhǔn)化工作已有一定基礎(chǔ),但尚未形成全國統(tǒng)一的標(biāo)準(zhǔn)化體系。標(biāo)準(zhǔn)不統(tǒng)一、數(shù)據(jù)不互認(rèn)的現(xiàn)象依然存在,這影響了部門之間、地區(qū)之間的政策銜接和數(shù)據(jù)共享
-
強(qiáng)生醫(yī)療科技任命中國區(qū)新總裁;原啟生物CAR-T療法獲FDA快速通道資格
強(qiáng)生在華人事調(diào)整持續(xù)進(jìn)行。 7月15日,強(qiáng)生公司宣布,周敏濤將擔(dān)任其醫(yī)療科技中國區(qū)總裁,并向強(qiáng)生醫(yī)療科技亞太區(qū)主席Vishnu Karla匯報(bào)工作。同時(shí),周敏濤也成為了強(qiáng)生醫(yī)療科技亞太區(qū)領(lǐng)導(dǎo)團(tuán)隊(duì)的一員
-

腫瘤藥物研發(fā)“地震”?當(dāng)FDA愈發(fā)重視OS
如何證明一款在研腫瘤藥物的療效?延長(zhǎng)患者生存期(OS)必然是核心目標(biāo)。 不過,由于研發(fā)技術(shù)的發(fā)展,腫瘤患者的生存期顯著延長(zhǎng),因此實(shí)驗(yàn)組患者總生存期數(shù)據(jù)的獲得周期也被顯著拉長(zhǎng)。 這對(duì)于亟需新治療手段的腫瘤患者來說,或許等不及
-
被FDA撤銷加速審批腫瘤藥物的經(jīng)驗(yàn)教訓(xùn)
前言 在過去的十年里,美國食品藥品監(jiān)督管理局(FDA)和歐洲藥品管理局(EMA)正在為實(shí)現(xiàn)盡快為患者提供新型治療的目標(biāo)做出努力。FDA使用了加速審批(AA)計(jì)劃,該計(jì)劃允許在臨床研究中使用替代終
-
FDA引發(fā)的蝴蝶效應(yīng):全球監(jiān)管機(jī)構(gòu)加強(qiáng)CAR-T審查
FDA作為全球醫(yī)藥監(jiān)管的標(biāo)桿,擁有世界級(jí)權(quán)威和聲望。因此,其一舉一動(dòng),也成為全球監(jiān)管機(jī)構(gòu)的風(fēng)向標(biāo)。 去年11月28日,F(xiàn)DA宣布調(diào)查已上市的CAR-T療法是否會(huì)在極少數(shù)情況下導(dǎo)致T細(xì)胞惡性腫瘤的事件,就引發(fā)了蝴蝶效應(yīng): FDA的動(dòng)作,引起了全球監(jiān)管機(jī)構(gòu)的關(guān)注
-
未獲FDA批準(zhǔn),胃癌明星靶點(diǎn)FIC藥物遭遇黑天鵝
跨過終點(diǎn)的臨門一腳,zolbetuximab暫時(shí)還不能落下。 1月9日,安斯泰來宣布,由于第三方生產(chǎn)工廠存在未解決缺陷,不能在1月12日的PDUFA日期前批準(zhǔn)zolbetuximab上市。 也就是說,還需要整改生產(chǎn)問題,zolbetuximab才能拿下FIC藥物的光環(huán)
-

國產(chǎn)EGFR ADC的進(jìn)擊,從斬獲FDA肺癌“快速通道資格”開始?
國內(nèi)藥企的崛起,正在逐漸改變著全球創(chuàng)新的格局。至少,在個(gè)別領(lǐng)域,中國藥企已具備爭(zhēng)奪話語權(quán)的可能。 EGFR靶點(diǎn)就是如此。今年以來,在EGFR ADC領(lǐng)域,國內(nèi)藥企不斷帶來驚喜,先是百利天恒的重磅BD,又是復(fù)宏漢霖在強(qiáng)手如云的肺癌領(lǐng)域拿到FDA快速通道資格
-

有種霸權(quán)叫作FDA:對(duì)醫(yī)藥“慕強(qiáng)效應(yīng)”的思考
本文系基于公開資料撰寫,僅作為信息交流之用,不構(gòu)成任何投資建議。 如果一個(gè)火星人來地球開辦一家醫(yī)藥公司,且這家公司只能在一個(gè)國家經(jīng)營(yíng)業(yè)務(wù),那么這個(gè)火星人會(huì)將公司開設(shè)在哪里呢?答案顯而易見會(huì)是美國。 美國人口僅占全球的4.5%,但醫(yī)療市場(chǎng)份額卻達(dá)到了全球的40%
-
一天兩款基因療法上市,F(xiàn)DA的“陽謀”
12月8日,注定是載入基因療法史冊(cè)的一天。 當(dāng)日,F(xiàn)DA正式批準(zhǔn)福泰制藥與CRISPR Therapeutics共同研發(fā)的基因編輯藥物Casgevy上市。 這意味著,CRISPR基因編輯療法獲得了全球醫(yī)藥監(jiān)管標(biāo)桿的認(rèn)可,為其后續(xù)全球推廣奠定了扎實(shí)的基礎(chǔ)
-

-
三星生物遭FDA抨擊,CXO擴(kuò)張與質(zhì)量沒有二選一
近些年來,國內(nèi)Biotech的快速發(fā)展離不開CXO的助力。但太過于依賴CXO或許也不是一件好事。因?yàn)椋珻XO也難免有翻車的時(shí)候。 最近,處于擴(kuò)張期的三星生物就遭遇了翻車。 在剛剛過去的8月和9月,
-

杜絕超適應(yīng)癥適用,F(xiàn)DA禁止網(wǎng)絡(luò)違規(guī)銷售GLP-1
狂飆的減重藥,被FDA按下了減速鍵。 近日,F(xiàn)DA對(duì)兩家藥物在線供應(yīng)商出具警告信函,直指司美格魯肽和替澤帕肽的超適應(yīng)癥用于減重的亂象。在FDA的威壓下,一家藥物在線供應(yīng)商已經(jīng)停止這兩款藥物的銷售。 在國內(nèi),GLP-1藥物超適應(yīng)癥使用的情況同樣屢見不鮮
-

-
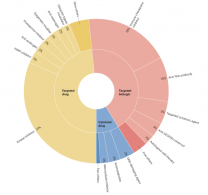
21世紀(jì)FDA癌癥藥物批準(zhǔn)的趨勢(shì)
前言 人們對(duì)癌癥治療藥物的研究可以追溯到20世紀(jì)初,然而第一批廣泛使用的化療產(chǎn)品是在第二次世界大戰(zhàn)期間的化學(xué)毒物研究中發(fā)現(xiàn)的。1949年,美國食品和藥物管理局(FDA)首次批準(zhǔn)癌癥的化學(xué)療法,即氮芥用于治療霍奇金淋巴瘤
-
阿斯利康王磊:中國業(yè)務(wù)分拆是謠言;馴鹿生物CD19單抗獲FDA批準(zhǔn)臨床
阿斯利康對(duì)網(wǎng)傳中國業(yè)務(wù)拆分消息表態(tài)。 昨日,《金融時(shí)報(bào)》稱,幾個(gè)月前,隨著地緣政治緊張局勢(shì)的加劇,阿斯利康已經(jīng)制定了剝離其中國業(yè)務(wù)并在港交所單獨(dú)上市的計(jì)劃。 對(duì)此,阿斯利康全球執(zhí)行副總裁、國際業(yè)務(wù)及中國總裁王磊今日向媒體回應(yīng)稱,該消息為謠言,阿斯利康中國各項(xiàng)業(yè)務(wù)目前一切正常
-
Neuralink人腦植入物試驗(yàn)獲FDA批準(zhǔn)
文/陳根5月25日,美國企業(yè)家埃隆·馬斯克旗下的腦機(jī)交互技術(shù)公司Neuralink宣布,已獲得美國食品和藥物管理局(FDA)批準(zhǔn),可以啟動(dòng)大腦植入設(shè)備的人體臨床試驗(yàn)。據(jù)馬斯克介紹,Neuralink公
-
FDA局長(zhǎng):細(xì)胞和基因療法應(yīng)該發(fā)展更快;貝達(dá)藥業(yè)2022年扣非凈利潤(rùn)下降91%
日前,F(xiàn)DA局長(zhǎng)Robert Califf博士在國會(huì)聽證會(huì)上表示,基因和細(xì)胞療法領(lǐng)域應(yīng)有更快的進(jìn)展。Robert Califf博士指出,F(xiàn)DA的生物制品評(píng)價(jià)和研究中心計(jì)劃增添150~200人手,這將有助于加快產(chǎn)品審評(píng)的速度
-

FDA:?jiǎn)蝺r(jià)新冠mRNA疫苗下架;科濟(jì)制藥實(shí)體瘤CAR T獲批臨床
新冠疫苗正式迭代。4月18日,F(xiàn)DA修改了Moderna和輝瑞-BioNTech新冠雙價(jià)mRNA疫苗的緊急使用授權(quán),以簡(jiǎn)化大多數(shù)人的疫苗接種。單價(jià)Moderna和輝瑞-BioNTech新冠疫苗將不再獲準(zhǔn)在美國使用
-
推想腦卒中AI產(chǎn)品獲NMPA三類證,成國內(nèi)首個(gè)斬獲NMPA與FDA“中美雙認(rèn)證”產(chǎn)品
根據(jù)國家藥品監(jiān)督管理局官網(wǎng)信息,近日,推想醫(yī)療顱內(nèi)出血CT圖像輔助分診軟件正式獲批國家藥品監(jiān)督管理局(NMPA)醫(yī)療AI三類證,可對(duì)顱腦CT平掃影像進(jìn)行顯示、處理、測(cè)量出血體積,用于對(duì)超急性期、急性期顱內(nèi)出血患者的分診提示
-
海信超聲出海又一里程碑:拿下“最嚴(yán)苛的”FDA認(rèn)證
6月9日,海信超聲產(chǎn)品HD60系列成功取得國際最權(quán)威的美國FDA認(rèn)證,這是繼CE認(rèn)證后海信超聲的又一里程碑,不僅標(biāo)志著其可以進(jìn)入北美市場(chǎng),也將為進(jìn)入更多國家奠定了基礎(chǔ)。去年以來,海信超聲已亮相多場(chǎng)國外專業(yè)展會(huì)并獲得已經(jīng)成功進(jìn)入南非、印尼以及阿聯(lián)酋等中東非市場(chǎng)
最新活動(dòng)更多 >
-
即日-5.20立即下載>> 【限時(shí)免費(fèi)】物理場(chǎng)仿真助力生物醫(yī)學(xué)領(lǐng)域技術(shù)創(chuàng)新
-
6月25日立即預(yù)約>> OFweek 2026中國高端醫(yī)療器械產(chǎn)業(yè)關(guān)鍵技術(shù)系列在線會(huì)議-醫(yī)療電子及先進(jìn)醫(yī)用材料關(guān)鍵技術(shù)專場(chǎng)
-
精彩回顧立即查看>> OFweek 2026智慧醫(yī)院創(chuàng)新發(fā)展大會(huì)暨醫(yī)療機(jī)器人創(chuàng)新發(fā)展峰會(huì)
-
精彩回顧立即查看>> 深圳“OFweek 2026醫(yī)療機(jī)器人創(chuàng)新發(fā)展峰會(huì)“
-
精彩回顧立即查看>> OFweek2026智慧醫(yī)院創(chuàng)新發(fā)展大會(huì)
-
精彩回顧立即查看>> OFweek2026醫(yī)療器械技術(shù)系列在線會(huì)議-AI精準(zhǔn)醫(yī)療專場(chǎng)
- 高級(jí)日語客戶開發(fā)專員 艾美特電器(深圳)有限公司
- 功能維修 深圳市維爾晶科技有限公司
- 材料研發(fā)工程師 廣州黑格智造信息科技有限公司
- 激光技術(shù)項(xiàng)目總監(jiān) 嘉興艾可鐳光電科技有限公司
- 海外品牌分銷經(jīng)理(多地區(qū)/國家) 深圳綠米聯(lián)創(chuàng)科技有限公司
- AOI副經(jīng)理(J10699) 伯恩光學(xué)(惠州)有限公司
- 管培生 深圳市迪瑞達(dá)自動(dòng)化有限公司
- 銷售業(yè)務(wù)員 永盛昌科技(深圳)有限公司
- 產(chǎn)品經(jīng)理(系統(tǒng)產(chǎn)品工程師) 深圳奧尼電子股份有限公司
- 研發(fā)工程師 珠海科德電子有限公司





