中國CAR-T第一股今日登陸納斯達克,市值達47億美元
自此,JNJ-4528的研究進展也開始層層推進。在獲得FDA授予的孤兒藥資格,以及歐盟EMA授予的PRIME藥品認定后,2019年12月,楊森公司宣布,美國FDA授予該公司靶向B細胞抗原(BCMA)的CAR-T療法JNJ-4528突破性療法認定,用于治療經治多發性骨髓瘤患者。突破性療法認定將加快這一創新療法的開發和審評過程。
目前,全球正在注冊開展的CAR-T臨床試驗主要在中美兩國,大多處于臨床前期和臨床1-2期。據市場調研機構Coherent Market Insights此前統計,2018年至2028年,全球CAR-T細胞免疫治療市場的平均年復合增長率將達46.1%,其中北美和歐洲依舊是兩大主要市場。
不過,在當下的CAR-T制藥發展領域上,仍有不少需要應對的風險。除了臨床上普遍會產生的細胞因子風暴,還有一個發展瓶頸便是細胞產品的制備CMC。在制備CMC上,就連BMS也未能做到令人滿意。在2020年的ASCO會前,BMS原本要著重“宣傳”的產品便因數據問題而被FDA拒批。
目前,JNJ-4528的Ⅱ期驗證性試驗仍于中國進行中。除了JNJ-4528,傳奇生物在細胞治療領域也布局了多條管線,針對非霍奇金淋巴瘤NHL、急性髓細胞性白血病AML、以及治療NHL的靶點為CD20同種異體CAR-T候選藥物等。
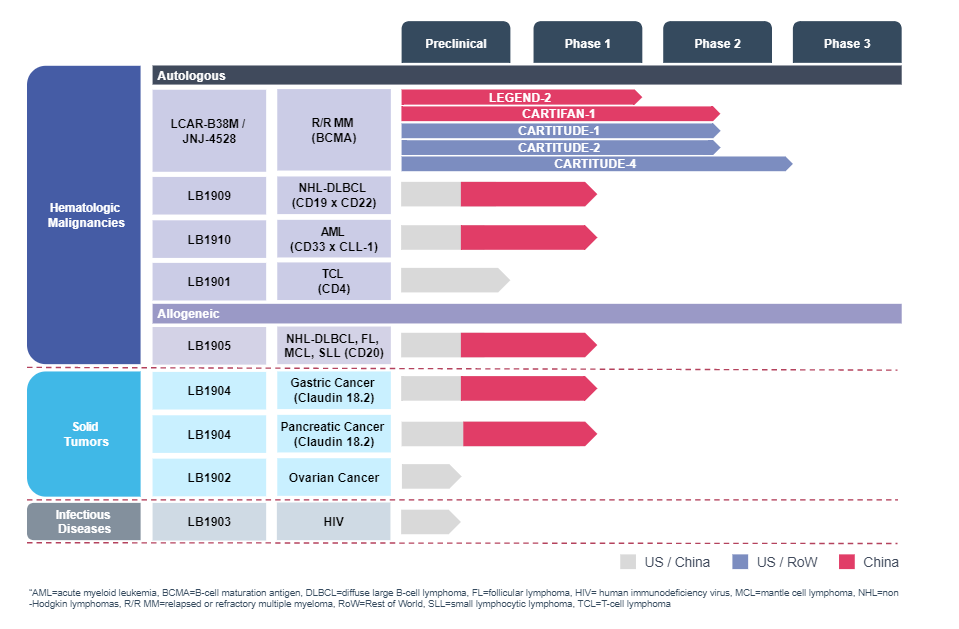
傳奇生物研發管線。圖源:傳奇生物官網
這些管線均為處于臨床早期的自體候選組合,其中進展最快的產品仍是JNJ-4528。傳奇生物預計于2020年下半年向FDA提交JNJ-4528適用于R/RMM治療的BLA(生物制品許可申請),并準備推動其在歐洲、中國、日本獲批上市。
由于還未有產品上市,傳奇生物的收入主要來自與楊森的合約收益。2019年年報顯示,報告期內,傳奇生物實現營收5726.4萬美元,同比增長16.5%,收入包括確認根據協議收到的預付款和里程碑付款。截至目前,楊森向傳奇生物支付了3.5億美元的預付費用和總計1.1億美元的里程碑付款。

請輸入評論內容...
請輸入評論/評論長度6~500個字
圖片新聞







 分享
分享












