突破藥研壁壘:病毒、脂質體、外囊泡、ADC
根據細胞外囊泡(EVs)的生物合成或釋放途徑,可以對囊泡進行分類:外泌體(exosomes)、微粒/微囊泡(microparticles/microvesicles)、凋亡小體(apoptotic body/bleb)、腫瘤小泡(large oncosomes),以及其他各種EV亞群。外囊泡膜可抵抗胞外環境核酸酶的降解作用,因此可作為小分子核酸藥物載體,這方面的應用已有大量文獻報道。
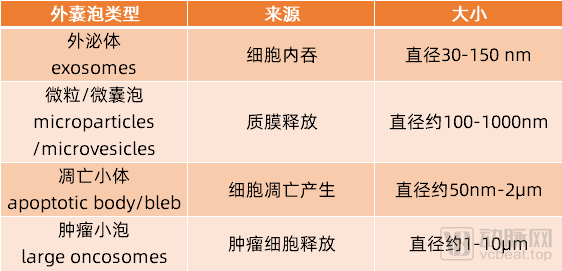
幾種外囊泡對比
目前,產業界用以載體開發的外囊泡(EVs)主要有三種:人源工程化外泌體、人類間充質干細胞(MSCs)來源的外泌體和紅細胞/血小板等無核細胞來源的外泌體。工程化外泌體因為可以修飾其靶向并且提升藥物裝載效率,目前是產業界的主流。MSCs來源的外泌體大約40-80nm大小,可以遞送20-30 bp微小RNA,紅細胞來源的外泌體由于受到紅細胞本身特質的影響最長可以攜帶30 kb的DNA。
2偶聯靶向遞送:自由搭配靶頭,高壁壘“生物導彈”
與載體遞送方式不同的是,偶聯靶向技術是用一個Linker(連接子)將藥物和具備靶向遞送功能的分子相連接,形成的具有靶向遞送功能的偶聯藥物。最常見的如有ADC藥物,最早被開發應用為“生物導彈”,利用生物大分子(抗體)的特異性,定向把小分子毒素(非特異性)送到病灶(如癌細胞),實現特異性殺滅癌細胞,而不影響正常細胞。
ADC藥物的起源可以追溯到1980年,最初的設想是將單克隆抗體靶向治療與傳統化療相結合,使其在抗癌方面既具有靶向的高度選擇性,又具有化療的強大殺傷力。
目前,ADC藥物主要由抗體-Linker(連接子)-藥物三部分構成。其中,Linker連接的藥物多為細胞毒素,毒素相當于彈頭,用于殺傷腫瘤細胞;抗體相當于制導裝置,將毒素精確導航到靶點;連接子將抗體與毒素相連接,在細胞內釋放毒素。
根據Nature預測,2020年以前上市的10款ADC產品到2026年銷售總額將超過164億美元。國內ADC市場在2020年啟動,預計2024年及2030年分別達到74億及292億人民幣的規模,2024年至2030年復合年增長率為25.8%。
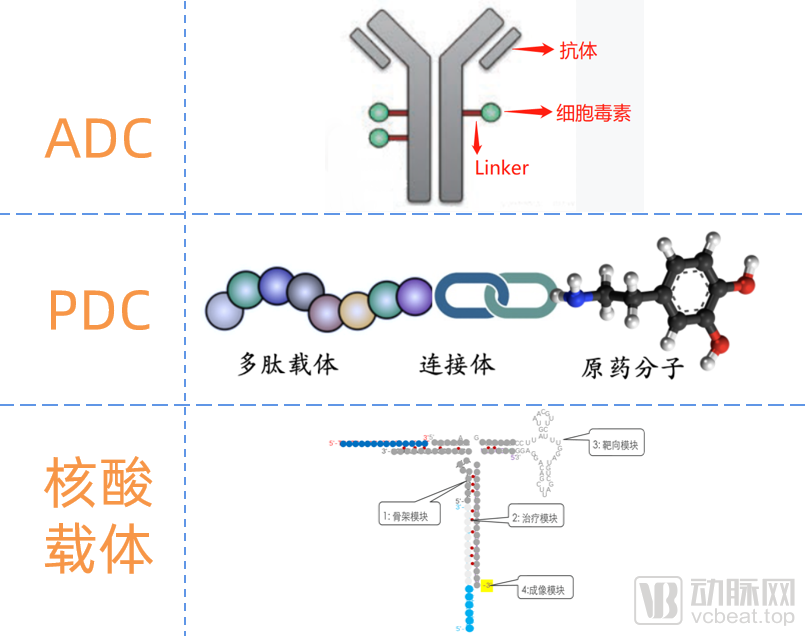
偶聯靶向遞送的幾種藥物形態
除了ADC,近年來還出現了多肽偶聯藥物(PDC),它和抗體偶聯藥物(ADC)類似,將其抗體-Linker(連接子)-藥物三部分中的“抗體”替換成了“多肽”,同樣可以具備靶向遞送功能。
PDC通過一個可分解的Linker將特定的多肽序列與細胞毒素共價結合,以提高局部細胞毒素濃度的形式靶向患病組織,減輕非疾病組織中的毒性效應,減輕不良反應,達到增效減毒的目的。
PDC整合了多肽的優勢,具有較小的分子量,可生物降解的同時不會引起免疫原性反應。通過修飾肽鏈的氨基酸序列,可改變PDC共軛疏水性和電離性質,解決水溶性差、代謝不及時等問題,同時促進細胞和組織通透性,攻克了小分子藥物由于理化性質欠佳在臨床開發中磨損率高的難題。一些特定的多肽載體還能克服腫瘤耐藥性,以及實現跨血腦屏障的藥物遞送。此外,相比于ADC技術,多肽偶練藥物PDC具有多種產業性優勢,例如更好的均一性,更低的生產成本和周期等。
不止ADC、PDC藥物可以作為“生物導彈”,臨床上還有抗體細胞偶聯藥物(ACC)、病毒樣藥物偶聯物(VDC)、抗體片段偶聯藥物(FDC)、抗體寡核苷酸偶聯物(AOC)、抗體免疫刺激偶聯物(ISAC)、抗體生物聚合物偶聯物(ABC)等偶聯藥物都可以實現遞送功能,但在這些領域產業研究比較少,所以本文不做過多解讀。
除了偶聯藥物,還有一些直接提供“連接體(Linker)”的遞送技術。例如通過設計組裝核苷酸形成特定藥物載體,使其與目標分子(包括具有靶向功能的大分子)的底層核酸序列偶聯,成為具備特定靶向遞送功能的核酸藥物。
相較于ADC、PDC藥物,納米核酸載體能夠實現多靶向適配體掛載,提升適配體介導藥物與靶細胞特異性結合;通過接頭設計確保靶向適配體不折疊,立體構象完整,保證了適配體介導的特異性和親和力;且靶向適配體和藥物整體分子量比值合理,提高了適配體介導藥物與靶細胞特異性結合幾率。納米核酸載體可以以序列延展方式掛載核苷酸片段和大部分N環類化藥等。
國內藥物遞送先行者:藥企們都使用哪些遞送技術?
了解了遞送技術的多種多樣,那么國內有哪些企業正在這個賽道發力呢?
首先,從病毒載體方面來看,基本上國內從事基因治療的藥企普遍采用都是病毒載體,包括有奧源和力、至善唯新、輝大基因、信念醫藥、安龍生物等近20家國內藥企正在使用病毒載體進行基因療法開發。
另一方面,國內也有不少提供專業病毒包裝技術服務的CRO/CDMO,例如有源興基因、吉凱基因、和元基因、白澤生物、漢恒生物、賽業生物等10余家企業,都能輸出品類多樣的臨床用病毒載體。

值得介紹的是,本導基因自主研發的一種類病毒(VLP)遞送技術,遞送載體是一種介于病毒載體與非病毒載體之間的類病毒體,利用mRNA莖環結構與噬菌體衣殼蛋白特異識別的原理,通過病毒工程技術,將病毒和mRNA兩者的優點完美地結合起來,創造了新型遞送技術VLP-mRNA。類病毒載體一方面借助了病毒的外殼,使得其感染細胞的效率特別高,另一方面,則基于mRNA的自身瞬時性的特點,能讓基因編輯治療更加安全可控,降低脫靶效應。據悉,本導基因的VLP已經進入了臨床IIT階段。
與病毒載體和基因治療的強關聯不同,脂質體(LNP)作為遞送載體,與之關聯的不僅有前沿的mRNA疫苗,還有各類抗癌化療藥物,以及對藥物緩釋、藥物吸收有需求的臨床藥物都可以采用脂質體(LNP)作為遞送載體。
例如,競諾擇生物在基礎的脂質體(LNP)技術之上,創新研發了一種“多藥脂質體技術”,通過控制脂質體的載藥量和釋放速度,在保證療效的前提下降低藥物副作用;再通過修飾脂質體的表面,提高脂質體的靶向性,控制藥物在體內的分布和作用時間。該技術能夠讓聯合使用的藥物在體內的分布和半衰期發生變化,藥物在體內分布將趨向一致,以此改善藥物的代謝行為,增強聯合化療的協同作用,彌補現有方法的不足,提高治療效果。
不過圍繞脂質體(LNP)最前沿的研究還是建立在核酸疫苗之上,因為疫苗注射本身對其靶向性要求不高,所以成為核酸疫苗注射首選的藥物載體。在國內,深信生物、傳信生物圍繞RNA藥物(多為疫苗)展開的研究都是借助了脂質體(LNP)作為遞送載體,脂質體(LNP)成為傳染疾病mRNA疫苗最具潛力的遞送技術。
其中,深信生物采用的脂質體(LNP)是一種可離子化陽離子的脂質納米粒,內部可以很好負載核酸藥物,相對于AAV病毒載體,這種載體具備更大的遞送空間和更好的重復遞送性。
另外,值得一提的還有渤因生物,該公司圍繞核酸(DNA)藥物/基因治療展開創新藥研發,采用的卻不是病毒載體,而是一種非病毒可重復遞送的藥物載體。據了解,該非病毒載體正是基于脂質體(LNP)基礎之上研發而來針對DNA遞送特異優化的創新載體。
其次在外囊泡載體方面,目前國內主要有恩澤康泰、博泌生物、宇玫博生物等企業正在做相關研究。其中,恩澤康泰主要是基于外囊泡中外泌體一類型作為大分子遞送載體,通過工程化改造的方式對外泌體進行改性,大幅提高了外泌體攜帶特定有效成分,包括多肽、蛋白質、核酸藥物的載量,并實現特定器官的選擇性遞送。
而博泌生物采用的是紅細胞外囊泡(RBCEV)載體遞送,公司先從O型血捐獻者的血液中分離紅細胞,在體外誘導使其分泌RBCEVs,然后經過純化得到高純度的RBCEVs。RBCEV可以裝載多達30kb的DNA片段,以及mRNA、反義寡核苷酸、siRNA等其他核酸藥物。由于紅細胞自身沒有細胞核和線粒體,也保證了分泌后的RBCEVs中核酸量含量極少,形成天然的空白核酸運載載體。
除了前文提及的載體制劑遞送,中國從事ADC藥物研發的企業超過20家,包括有榮昌生物、樂普生物、康諾亞、嘉和生物等;從事PDC藥物研發的另有安醫生命科技(N1 Life)、泰爾康醫藥、主流生物、同宜醫藥、盛諾基醫藥等不到10家,該領域在國內還處于開發的洼地,研究公司并不多見。
例如,安醫所使用的Linker連接的多肽不僅能夠靶向腫瘤微環境,使藥物腫瘤形成富集,讓腫瘤組織內部藥物富集,從而提高藥效濃度、藥物吸收效率,降低藥物毒副作用,同時還利用多肽載體克服腫瘤的多重耐藥性,甚至擴大原始藥物的適應癥;康源久遠用linker鏈接PEG化的毒素,克服了傳統ADC耦聯技術的隨機性缺陷。
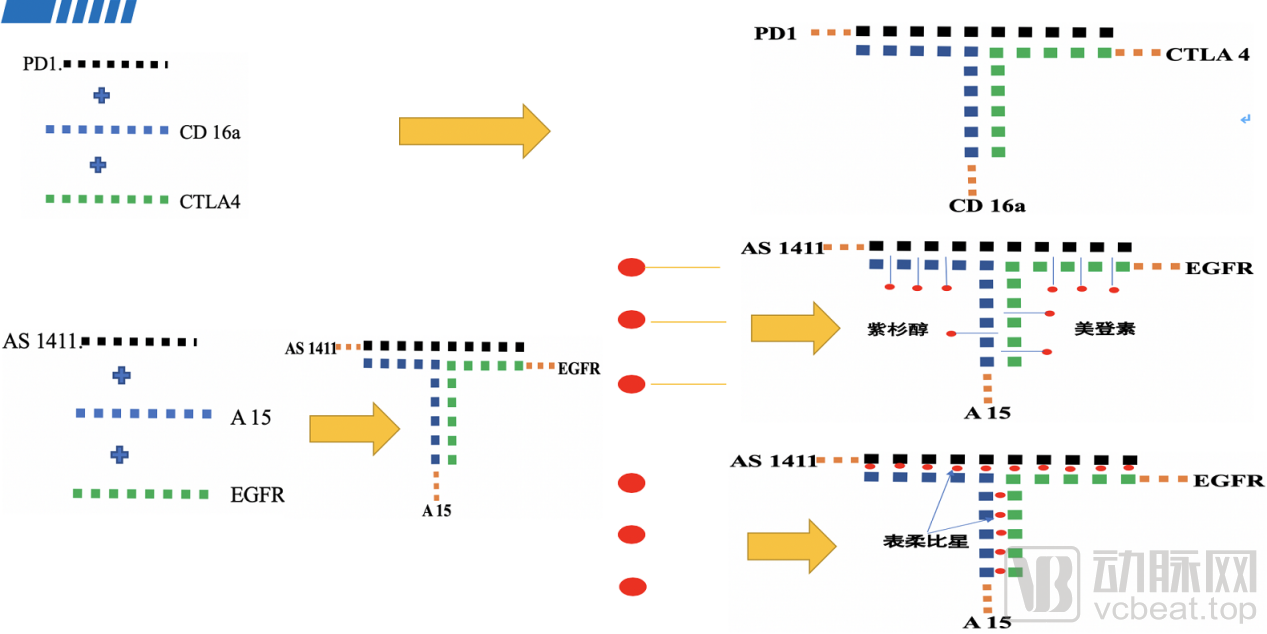
百藥智達的納米核酸藥物合成工藝
最后,值得介紹的還有一家專門從事遞送技術服務的藥企——百藥智達,該公司以核苷酸和修飾物為材料,仿生tRNA人工合成多條寡核苷酸RNA或DNA鏈,遵循堿基配對原理自主裝配成T型藥物載體系列;該載體動態粒徑約10nm(掛載藥物和靶向后約15nm),呈穩定超螺旋結構立體構象,具有優良熱力學、酸堿、血液生理、酶學穩定性;同時,百藥智達開發出系列序列延展、綴合、偶合方法,可以高效掛載各類靶頭及藥物效應分子,靈活成藥。
后記:沒有最好的載體,只有最適合的遞送技術
遞送技術在醫療產業中是一個非常大的盤子,從我們前文的研究可以看到,每一種遞送技術幾乎都有與之對應的契合的研發藥物。例如,核酸藥物最常見的是采用病毒載體,究其緣由是病毒載體的感染能力高、宿主范圍廣、同時表達多個基因等優勢都很適用于核酸藥物的運載。
當然,圍繞病毒載體本身的短板,也成為前沿科學家們致力于克服的地方,病毒的不可重復遞送性、隨機整合風險等,也就誕生出了諸如類病毒(VLP)載體類型,以及像渤因生物一樣嘗試用非病毒載體克服AAV病毒短板進行基因治療的企業。
提到非病毒載體,脂質體(LNP)則成為產業的寵兒,基于被遞送藥物的屬性差異,藥企開始圍繞脂質體進行的各類升級,以高效適應遞送目標藥物,納米脂質體、陽離子納米乳、多藥脂質體等,成為產業發展的一大方向。由于脂質體(LNP)的非主動靶向性,目前成為核酸疫苗的首選遞送技術,強大的可離子化磷脂化學結構改造優化能力,以及解速度快,產量高等優勢,未來的應用前景巨大。
相較病毒和脂質體(LNP)而言,天然的外囊泡則可以被認為最前沿的第三代遞送技術。不僅易于設計靶向性,還能天然運載大分子,且低免疫原性,有望彌補現有遞送技術的不足,成為獨具優勢的給藥系統。然而,目前國內從事該領域的企業并不多,技術工藝也需要進一步完善。不過據業內人士透露,目前國內諸多藥企已經開始嘗試使用外囊泡遞送技術替代原有遞送方式,以提高藥物遞送效率等相關屬性。
最后是我們提及小分子藥物,可以偶聯單抗、多肽等形成靶向藥物,定向導航到病變(多為腫瘤)部位。與此同時,連接小分子藥物和大分子單抗/多肽的linker也可以成為科學家們優化的對象,以及如何提高這些偶聯藥物的均一性,也是前沿藥企需要解決的問題。所以,也有藥企嘗試直接構建核酸載體,將需要運載的藥物直接“回歸”到核苷酸序列本身,與納米核酸載體相連形成穩定的核酸復合物,解決藥物遞送均一性問題。
綜上所述,醫藥界對遞送技術的探索是永無止境的,永遠在研究更為高效、完美的遞送系統。遞送系統與醫藥是協同發展,遞送在醫藥領域無處不在,也將是醫藥產業發展中一個永恒的話題。
特別鳴謝:
百藥智達合伙人 魏鴻
競諾擇生物創始人 馮皓
恩澤康泰CEO 孔關義
深信生物創始人 李林鮮
渤因生物創始人 潘雨堃
Carmine Therapeutic聯合創始人 史家海
科凝生物創始人 余渝
本導基因創始人 蔡宇伽
安醫生命科技(N1 Life)創始人 臧曉羽
康源久遠CEO 劉樹民
和度生物......
作者:王嬋

請輸入評論內容...
請輸入評論/評論長度6~500個字
圖片新聞







 分享
分享












